Molekuła i różne stany materii
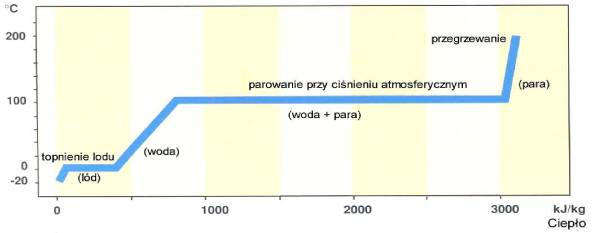
Atomy połączone ze sobą poprzez wiązania chemiczne nazywane są molekułami. Są tak małe, że np. $ 1 mm^3 $ powietrza przy ciśnieniu atmosferycznym zawiera ok. $ 2,55 \times 10^{16} $ molekuł. Materia może zasadniczo znajdować się w czterech różnych stanach: stanie stałym, stanie płynnym, stanie gazowym i stanie plazmy. W stanie stałym ciasno upakowane w sieci molekuły połączone są silnymi wiązaniami. W każdej temperaturze powyżej zera absolutnego dochodzi do pewnego ruchu molekuł, w stanie stałym w formie drgań wokół położenia równowagi tym szybszych im wyższa jest temperatura. Jeżeli substancja w stanie stałym zostanie podgrzana tak, że stała, sztywna struktura sieciowa nie może powstrzymać ruchu molekuł to molekuły stają się swobodne, substancja topnieje i przechodzi w stan płynny.
Jeżeli substancja jest w dalszym ciągu podgrzewana to wiązania molekularne zostają zerwane i substancja przechodzi w stan gazowy, molekuły poruszają się w różnych kierunkach mieszając się z innymi gazami obecnymi w danym pomieszczeniu. Jeżeli molekuły gazu zostają schłodzone tracą swoją szybkość i powtórnie wiążą się ze sobą. Rozpoczyna się proces kondensacji. Jednakże jeżeli molekuły gazu są dalej podgrzewane to rozpadają się one na pojedyncze cząstki i tworzą plazmę elektronów i jąder atomowych.
Bibliografia dodatkowa
- Atlas Copco: Technika sprężonego powietrza - poradnik. Atlas Copco Airpower NV. ISBN 9789081535809.